[서울신문]
생후 5개월 된 아기 엄마인 A씨는 지난달 모유가 잘 나오지 않아 병원에서 진료를 받고 ‘돔페리돈’ 성분이 함유된 약을 처방받았다. 그런데 최근 뉴스를 보다가 돔페리돈 성분이 돌연사를 일으킬 수 있다는 보도를 보고 걱정이 되기 시작했다. 특히 이미 먹은 약으로 인해 아기에게 영향을 미칠 수 있다는 사실이 가장 큰 걱정이다. A씨는 “돔페리돈이 신생아에게 심장질환 등의 부작용을 발생시킬 수 있다는 것을 알았다면 처방받지 않았을 것”이라면서 “병원에서는 처방받은 약이 안전하다고 하지만 여전히 걱정되는 게 사실”이라고 말했다.
8일 통계청에 따르면 국민 1인당 연간 의약품 판매액은 2012년 43만 4679원에서 2013년 44만 9154원, 2014년 46만 9329원으로 꾸준히 늘고 있다. 약을 복용하는 절대량이 많아지면서 약품의 안전성이나 효능에 대한 논란 또한 늘고 있다.
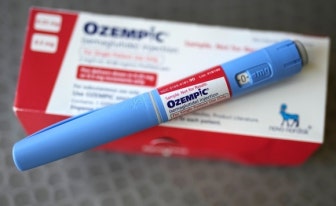
지난달 초 국회 보건복지위원회 전혜숙 더불어민주당 의원이 국정감사를 통해 문제를 제기하면서 시작된 돔페리돈의 안전성 논란은 한 달이 넘는 지금도 ‘현재진행형’이다. 돔페리돈은 구토 증상을 완화하는 성분이 있어 위장약 등에 쓰인다. 복용 시 일부 환자들에게 모유를 촉진시키는 효과를 보이기도 하는 것으로 알려져 모유량이 적은 산모들에게 비급여(식약처에서 정해준 허가목적 외 목적으로 처방하는 것) 처방으로 약을 복용토록 해 왔다. 전 의원은 돔페리돈이 심장질환 부작용이 있어 미국에서는 식품의약국(FDA) 허가를 받지 않았고 유럽의약품청(EMA)에서도 2014년 4월 제한적 사용권고가 났음에도 우리나라에서는 지난해 3월부터 12월까지 10개월 동안 7만 8361건의 돔페리돈이 처방됐다고 주장했다.
최근 식약처에서 치주질환 치료제로 판매됐던 동국제약 ‘인사돌’과 명인제약 ‘이가탄’의 효능 효과를 ‘치주치료 후 치주염의 보조치료제’로 바꾼 것 역시 소비자들에게 혼란을 가중시키고 있다. 인사돌과 이가탄에 대한 치료 효과 논란은 2013년 처음 불거졌으나 이에 대한 별다른 설명이 없다가 3년이 지난 뒤에야 바뀌었다. 동국제약과 명인제약 측은 보조치료제로 바뀐 것에 대해 “식약처가 공식적으로 약의 효능을 인정한 것”이라면서 “오히려 그동안의 논란을 확실하게 해결했다”는 입장이다. 식약처 관계자는 “규정에 따라 약품 제조업체들에 임상 재평가를 실시한 뒤 전문가들의 의견을 거쳐 결정하느라 시일이 좀 걸린 것”이라고 설명했다. 하지만 결국 식약처가 논란 이후 3년 만에 인사돌과 이가탄을 보조치료제로 바꾸면서 앞서 치료제로 알고 인사돌이나 이가탄을 장기 복용했던 치주염 환자들은 이에 대한 책임을 물을 곳이 없어졌다.
미용 목적으로 쓰이고 있는 보툴리눔톡신 균주(보톡스)를 둘러싼 업체 간 갈등도 마찬가지다. 지난달 14일 국내 보톡스 업체인 메디톡스가 휴젤과 대웅제약의 보톡스 균주 출처에 대한 의혹을 제기하면서 시작된 갈등이 한 달 가까이 지속되고 있지만 이를 관장하는 질병관리본부는 이제서야 부처 간 협의 자리를 만들겠다고 밝힌 상태다.
환자들은 이처럼 약품의 안전성과 효능 등에 대해 논란이 커지는 상황에서 이에 대한 불안감을 해소해 줘야 할 당국이 너무 소극적으로 움직이고 있다고 불만을 토로한다. 지난해 수유 과정에서 돔페리돈을 처방받아 복용했다는 한 산모는 “현재는 문제가 없지만 나중에 돔페리돈 복용으로 인해 혹여라도 이상이 나타날 경우 이에 대한 보상을 어떻게 받아야 하는지 걱정”이라면서 “어느 곳에서도 명확한 설명을 해 주는 곳 없이 의사가 단순히 문제가 없다고만 하면 믿고 복용해야 하는 건지 답답하다”고 말했다. 의료·보건업계에 오랜 기간 종사해 온 한 관계자는 “의약품의 경우 의사나 약사, 제약업체 등 모두가 각자의 이해관계가 걸려 있기 때문에 사실상 의약품의 안전성이나 효능 등에 대해 객관적으로 말해 줄 수 있는 곳은 정부 당국이 유일하다”고 말했다.
대한의사협회 회장을 지낸 노환규 하트웰의원 원장은 “의약품은 약을 판매한 뒤에 그에 대한 부작용을 모니터할 수 있는 시스템이 필요하다”면서 “선진국의 경우 환자들이나 약사, 의사 등이 특정 약품에 대한 부작용을 발견했을 경우 당국에 직접 신고할 수 있는 정부기관이 상시 운영되고 있지만 우리나라는 약품에 대한 부작용이 있을 때 마땅히 신고할 수 있는 실질적인 창구가 없다”고 말했다. 이에 식약처 관계자는 “2012년부터 한국의약품안전관리원을 통해 의약품 부작용을 신고받고 있다”고 설명했다.
박재홍 기자 maeno@seoul.co.kr
▶ [웰 메이드 N], 재미있는 세상[나우뉴스]
▶ [인기 무료만화] [페이스북]
ⓒ 서울신문(www.seoul.co.kr), 무단전재 및 재배포금지